Pandemia
Vacina para adolescentes: Janssen realiza estudo, Coronavac aguarda aprovação
Com a aceleração da vacinação dos adultos contra a Covid-19 no Brasil e o sinal positivo do Ministério da Saúde para que seja feita a aplicação de doses também em menores de 18 anos em breve – o que o governo federal estima para setembro- cresce a expectativa de adolescentes e crianças (e de seus pais) para que, em algumas semanas, todos começam a receber uma dose.
Na quinta-feira (29), o presidente Jair Bolsonaro sancionou lei que inclui crianças e adolescentes com deficiência permanente ou com comorbidade como grupo prioritário para a vacinação contra a Covid-19, assim como gestantes e lactantes e pessoas privadas de liberdade.
Pfizer
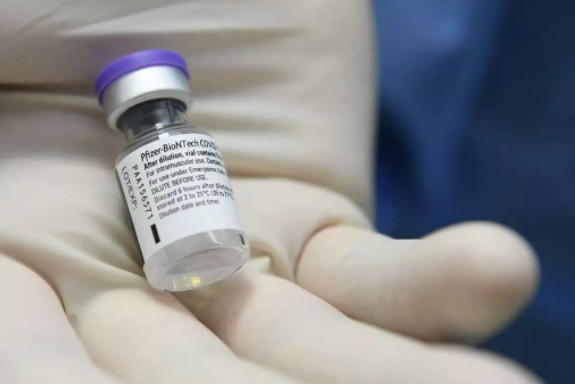
Única vacina que já possui autorização da Anvisa para aplicação em adolescentes, desde 11 de junho, o imunizante da Pfizer é indicado para o público acima de 12 anos. A vacina já está em uso para menores de 18 anos em diferentes cidades, como Niterói, no Rio de Janeiro, que se anteciparam ao governo federal. Os estudos foram desenvolvidos fora do Brasil e avaliados pela Anvisa. As solicitações da Pfizer/BioNTech foram baseadas em resultados “de um estudo clínico de fase 3 em menores de 12-15 anos de idade”, que mostrou “100% de eficácia” da vacina, segundo seus fabricantes disseram à AFP. Segundo a agência de notícias, a Pfizer/BioNTech também testa crianças de 5 a 12 anos.
Coronavac
Na sexta-feira (30), a Anvisa recebeu solicitação do Instituto Butantan para ampliar a faixa etária da vacina Coronavac. O laboratório quer incluir o público de crianças e adolescentes entre 3 a 17 anos na bula. Atualmente, a vacina está autorizada para uso emergencial no Brasil para pessoas com 18 anos de idade ou mais, desde o dia 17 de janeiro. No caso da Coronavac, estudos em menores de 18 anos foram conduzidos fora do país.
Janssen
O laboratório Janssen recebeu autorização da Anvisa para realizar estudos de sua vacina com menores de 18 anos no Brasil. Eles estão em condução atualmente. A reportagem fez contato com a Johnson & Johnson solicitando detalhes, mas não recebeu retorno. Esta vacina foi aprovada pela Organização Mundial de Saúde (OMS) e também pela Anvisa, no Brasil, em 31 março, para uso em adultos.
Astrazeneca
Em relação à Astrazeneca, a Fiocruz informou que “ainda não há estudos da Fiocruz em curso para avaliar a eficácia da vacina em menores de 18 anos”.
Fonte: O Tempo
Foto: Piero Cruciatti/Pool/AFP
Clique aqui e faça parte de nosso grupo de whatsapp
Clique aqui e siga-nos no instagram
Clique aqui e siga-nos no facebook
JORNAL O POPULAR – A NOTÍCIA COM DEVE SER

































